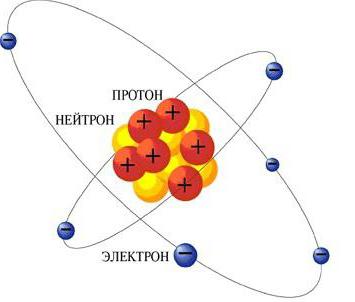
Atomu kodola struktūra un maksa
Fakts, ka visi posteņi sastāv no elementārasdaļēji tika pieņemtas arī Senās Grieķijas zinātnieki. Bet ne šo faktu pierādīšanai, ne arī tam, lai atspēkotu, šajās dienās nebija iespējas. Jā, un atomu īpašības senatnē varēja tikai uzminēt, pamatojoties uz saviem dažādu vielu novērojumiem.

Molekulu, atomu un to struktūras pētījums bijatiek veltīti daudzu zinātnieku darbi. Fizika pakāpeniski nonāca mikrorajona pētījumos - elementārās daļiņas, to mijiedarbība un īpašības. Zinātnieki sāka domāt par to, kas ir atomu kodols, izvirzot hipotēzes un mēģinot tos pierādīt vismaz netieši.
Tā rezultātā pamatteorija bijaTiek pieņemts Ernest Rutherford un Niels Bohr ierosinātā atomenerģijas planētais modelis. Saskaņā ar šo teoriju, jebkura atoma kodola uzlāde ir pozitīva, savukārt tās orbītas rotē negatīvi lādējušos elektronus, galu galā padarot atomu elektriski neitrālu. Laika gaitā šo teoriju vairākkārt apstiprināja dažāda veida eksperimenti, sākot ar viena no tā līdzautoriem veiktajiem eksperimentiem.

Protams, mūsdienu pasaulē, nosakiet maksuPiemēram, alumīnija (vai jebkura cita elementa) kodols ir daudz vienkāršāks nekā 19. gadsimtā un vēl jo vairāk Senajā Grieķijā. Bet, radot jaunus atklājumus šajā jomā, zinātnieki dažreiz nāk pie pārsteidzošiem secinājumiem. Mēģinot atrast risinājumu vienai problēmai, elementārās daļiņu fizika saskaras ar jaunām problēmām un paradoksiem.

Tas ir ziņkārīgs, ka ilgi pirms pētījumaRutherfordas angļu ķīmiķis, ārsts pēc izglītības William Prout pamanīja, ka dažādu vielu īpatsvars ir šī ūdeņraža rādītājs. Pēc tam viņš ierosināja, ka visi pārējie elementi vienkārši sastāv no ūdeņraža dažā vienkāršākā līmenī. Piemēram, slāpekļa daļiņai ir 14 tādas minimālas daļiņas, 16 skābeklis utt. Ja šo teoriju mēs uzskatām par globālu mūsdienu interpretācijā, tad vispār tā ir pareiza.